深圳市默赛尔生物医学科技发展有限公司
6 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0
- 0
- 1
- 0
NK细胞培养试剂盒|自然杀伤细胞处理试剂盒
¥4500
推荐产品
公司新闻/正文
用嵌合抗原受体改造的NK细胞靶向B7-H3免疫检查点对非小细胞肺癌表现出强大的细胞毒性
830 人阅读发布时间:2022-12-05 16:15
研究内容:
1. B7-H3在人癌组织和细胞系中的表达
本研究采用流式细胞术和免疫共沉淀法,用抗B7-H3 IgG 8H9检测了B7-H3在不同癌细胞系中的表达。流式分析结果显示除B7-H3阴性细胞(Daudi)外,B7-H3高表达于例如A549,NCI-H23,HCC827,DLD-1,HCT-116,和MDA-MB-231等多种癌细胞表面。蛋白印迹结果进一步证实,8H9抗体从A549和NCI-H23而非Daudi的全细胞裂解液中免疫沉淀出约为100kDa的4Ig-B7- H3蛋白。免疫组化结果显示8H9抗体和商用抗B7-H3抗体在人非小细胞肺癌组织中检测到B7-H3,在肺正常组织中未见阳性染色。以上结果表明B7-H3在人实体瘤细胞系和组织中高表达。8H9抗体对B7-H3表现出较强的反应性,但对正常组织无交叉反应性,因此8H9抗体被选用于CAR的构建。
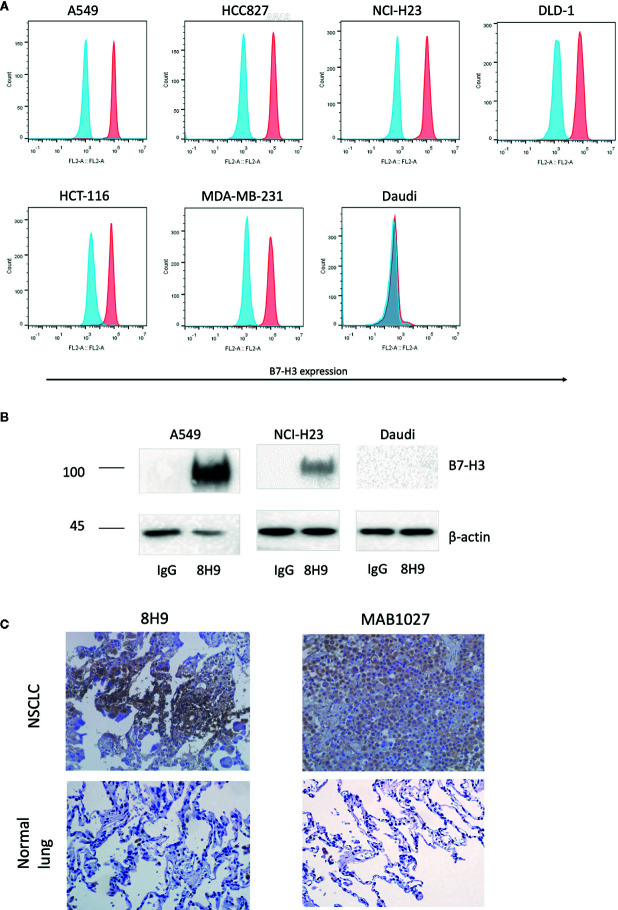 图1:B7-H3在肿瘤细胞系和原代人体组织上的表达
2. 携带抗B7-H3 CAR的NK-92MI细胞的生成
抗B7-H3 scFv由(G4S)3接头将抗B7-H3抗体8H9的轻链和重链可变区连接而成。抗B7-H3 CAR构建体由抗 B7-H3 scFv、CD8 TM 区、4-1BB和CD3 ζ 胞内结构域组成。将CAR DNA序列插入到与ZsGreen 共表达的pLVX慢病毒载体中,随后产生慢病毒颗粒并转导入人NK-92MI细胞中,转到效率为24.9%。经过几轮分选,表达CAR的NK-92MI细胞百分比超过了95%。抗B7-H3 CAR的表达用qPCR检测,结果显示,与未转导的NK-92MI细胞相比,CAR在转导的NK-92MI细胞中高表达。
图1:B7-H3在肿瘤细胞系和原代人体组织上的表达
2. 携带抗B7-H3 CAR的NK-92MI细胞的生成
抗B7-H3 scFv由(G4S)3接头将抗B7-H3抗体8H9的轻链和重链可变区连接而成。抗B7-H3 CAR构建体由抗 B7-H3 scFv、CD8 TM 区、4-1BB和CD3 ζ 胞内结构域组成。将CAR DNA序列插入到与ZsGreen 共表达的pLVX慢病毒载体中,随后产生慢病毒颗粒并转导入人NK-92MI细胞中,转到效率为24.9%。经过几轮分选,表达CAR的NK-92MI细胞百分比超过了95%。抗B7-H3 CAR的表达用qPCR检测,结果显示,与未转导的NK-92MI细胞相比,CAR在转导的NK-92MI细胞中高表达。

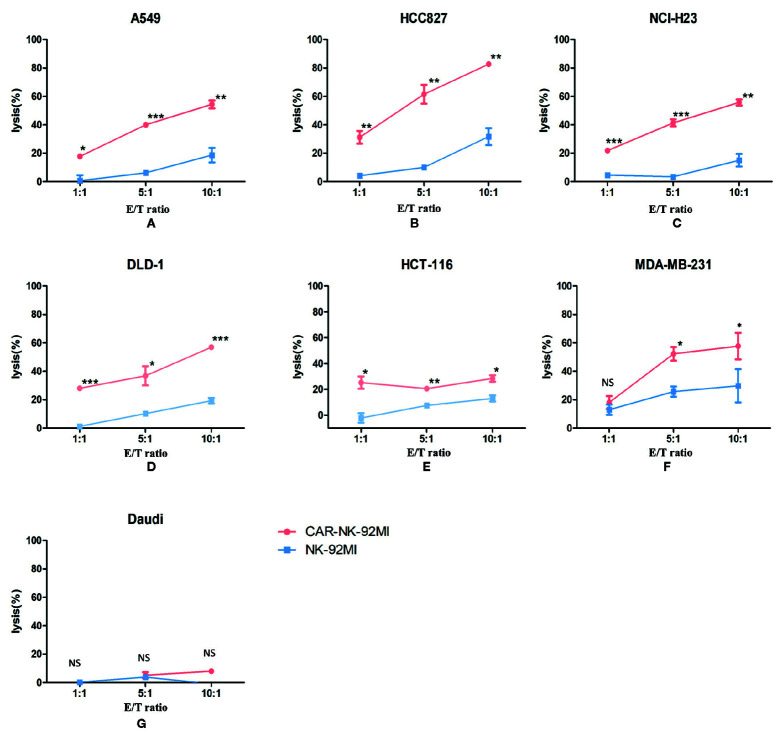 图3:B7-H3 CAR-NK-92MI 细胞对一组肿瘤细胞系的体外细胞毒性测定
4. CAR-NK-92MI细胞响应B7-H3阳性靶细胞的活化升高
NK细胞活化的一个标志是脱颗粒,其中裂解颗粒内容物(穿孔素和颗粒酶)被释放到靶细胞表面。CD107a、颗粒酶B、穿孔素是脱颗粒的三个主要标志物。为了进一步分析CAR-NK-92MI细胞的脱颗粒,我们通过流式细胞术分析了CD107a的表达和颗粒酶B、穿孔素的分泌。CAR-NK-92MI细胞分别与A549、NCIH23细胞以E/T为1:1共培养24h,结果显示,相比于未修饰的NK-92MI细胞,CAR-NK-92MI细胞表面CD107a的表达具有显著性差异。另外,B7-H3 CAR增强了在NK-92MI细胞脱颗粒中穿孔素、颗粒酶B的表达。在与靶细胞响应时,CAR-NK-92MI细胞中的颗粒酶B和穿孔素的水平显著上调。尽管A549细胞比NCIH23细胞表达更高水平的B7-H3,但是A549细胞中CD107a的水平似乎比NCIH23要低,这意味着溶细胞颗粒极化和脱颗粒不是由高于阈值的B7-H3密度决定的。我们假设不同受体控制两个细胞系的脱颗粒。因此,结果表明,脱颗粒激活在CAR-NK-92MI细胞的细胞毒性中起重要作用。
图3:B7-H3 CAR-NK-92MI 细胞对一组肿瘤细胞系的体外细胞毒性测定
4. CAR-NK-92MI细胞响应B7-H3阳性靶细胞的活化升高
NK细胞活化的一个标志是脱颗粒,其中裂解颗粒内容物(穿孔素和颗粒酶)被释放到靶细胞表面。CD107a、颗粒酶B、穿孔素是脱颗粒的三个主要标志物。为了进一步分析CAR-NK-92MI细胞的脱颗粒,我们通过流式细胞术分析了CD107a的表达和颗粒酶B、穿孔素的分泌。CAR-NK-92MI细胞分别与A549、NCIH23细胞以E/T为1:1共培养24h,结果显示,相比于未修饰的NK-92MI细胞,CAR-NK-92MI细胞表面CD107a的表达具有显著性差异。另外,B7-H3 CAR增强了在NK-92MI细胞脱颗粒中穿孔素、颗粒酶B的表达。在与靶细胞响应时,CAR-NK-92MI细胞中的颗粒酶B和穿孔素的水平显著上调。尽管A549细胞比NCIH23细胞表达更高水平的B7-H3,但是A549细胞中CD107a的水平似乎比NCIH23要低,这意味着溶细胞颗粒极化和脱颗粒不是由高于阈值的B7-H3密度决定的。我们假设不同受体控制两个细胞系的脱颗粒。因此,结果表明,脱颗粒激活在CAR-NK-92MI细胞的细胞毒性中起重要作用。
 图4:B7-H3 CAR-NK-92MI 细胞的脱粒和颗粒分泌
5. CAR-NK-92MI细胞在NSCLC移植瘤中的治疗效果
为了评估体内抗肿瘤活性,建立了A549细胞皮下模型。植入10天后,三组A549细胞移植瘤小鼠分别接受静脉注射CAR-NK-92MI细胞(5x10^6/剂)、未修饰NK-92MI细胞(5x10^6/剂)和PBS在第10、17、24、31天。结果显示,在实验结束时,相比于NK-92MI组和PBS组,CAR-NK-92MI组分别缩小肿瘤体积52.1%、63.8%。CAR-NK-92MI组的存活时间显著长于PBS组和NK-92MI组。因此CAR-NK-92细胞有效抑制肿瘤生长和荷瘤小鼠的生存期。
图4:B7-H3 CAR-NK-92MI 细胞的脱粒和颗粒分泌
5. CAR-NK-92MI细胞在NSCLC移植瘤中的治疗效果
为了评估体内抗肿瘤活性,建立了A549细胞皮下模型。植入10天后,三组A549细胞移植瘤小鼠分别接受静脉注射CAR-NK-92MI细胞(5x10^6/剂)、未修饰NK-92MI细胞(5x10^6/剂)和PBS在第10、17、24、31天。结果显示,在实验结束时,相比于NK-92MI组和PBS组,CAR-NK-92MI组分别缩小肿瘤体积52.1%、63.8%。CAR-NK-92MI组的存活时间显著长于PBS组和NK-92MI组。因此CAR-NK-92细胞有效抑制肿瘤生长和荷瘤小鼠的生存期。
 图5:用B7-H3 CAR-NK-92MI细胞治疗NSCLC异种移植瘤
实验结论:
在本研究中,我们构建了由4-1BB共刺激信号域和CD3ζ 结构域组成的第二代CAR,与目前临床使用的抗CD19 CAR-T细胞相似。本研究证实了抗B7-H3 CAR通过41-BB和CD3ζ 链的信号直接触发了NK细胞的溶解细胞功能。体外细胞毒性实验表明,CAR-NK-92MI细胞依据H7-B3的识别功能特异性地杀死肿瘤细胞。另外,CAR-NK-92MI细胞显著增强对所有B7-H3阳性细胞系的细胞毒性能力。抗B7-H3 CAR的重定向进一步增强了NK的活化和脱颗粒。脱颗粒是NK细胞活化的一个重要过程,它被触发脱颗粒释放溶解的颗粒分子,进而诱导靶细胞凋亡。除了穿孔素和颗粒酶B外,还观察到CD107a在CAR-NK-92MI细胞中显著上调。另外,在NSCLC移植瘤中,CAR-NK-92MI细胞显现出有效的抗肿瘤能力和延长荷瘤小鼠的生存时间。虽然CAR-NK-92MI缺乏长期的持久性,但是多次使用CAR-NK92MI细胞可以克服此缺点。因为辐射的CAR-NK-92MI细胞对于患者输注是确保安全所必须的,所以在CAR-NK-92MI细胞被应用于临床试验之前,我们需要进一步研究辐照对CAR-NK-92MI细胞内在特征的影响。
总之,B7-H3可作为NSCLC治疗的靶点。抗B7-H3 CAR-NK-92MI在体内和体外显示出显著的治疗效果。我们的研究支持开发CAR修饰的NK-92细胞作为过继癌症免疫治疗的一种选择。
图5:用B7-H3 CAR-NK-92MI细胞治疗NSCLC异种移植瘤
实验结论:
在本研究中,我们构建了由4-1BB共刺激信号域和CD3ζ 结构域组成的第二代CAR,与目前临床使用的抗CD19 CAR-T细胞相似。本研究证实了抗B7-H3 CAR通过41-BB和CD3ζ 链的信号直接触发了NK细胞的溶解细胞功能。体外细胞毒性实验表明,CAR-NK-92MI细胞依据H7-B3的识别功能特异性地杀死肿瘤细胞。另外,CAR-NK-92MI细胞显著增强对所有B7-H3阳性细胞系的细胞毒性能力。抗B7-H3 CAR的重定向进一步增强了NK的活化和脱颗粒。脱颗粒是NK细胞活化的一个重要过程,它被触发脱颗粒释放溶解的颗粒分子,进而诱导靶细胞凋亡。除了穿孔素和颗粒酶B外,还观察到CD107a在CAR-NK-92MI细胞中显著上调。另外,在NSCLC移植瘤中,CAR-NK-92MI细胞显现出有效的抗肿瘤能力和延长荷瘤小鼠的生存时间。虽然CAR-NK-92MI缺乏长期的持久性,但是多次使用CAR-NK92MI细胞可以克服此缺点。因为辐射的CAR-NK-92MI细胞对于患者输注是确保安全所必须的,所以在CAR-NK-92MI细胞被应用于临床试验之前,我们需要进一步研究辐照对CAR-NK-92MI细胞内在特征的影响。
总之,B7-H3可作为NSCLC治疗的靶点。抗B7-H3 CAR-NK-92MI在体内和体外显示出显著的治疗效果。我们的研究支持开发CAR修饰的NK-92细胞作为过继癌症免疫治疗的一种选择。
 图1:B7-H3在肿瘤细胞系和原代人体组织上的表达
2. 携带抗B7-H3 CAR的NK-92MI细胞的生成
抗B7-H3 scFv由(G4S)3接头将抗B7-H3抗体8H9的轻链和重链可变区连接而成。抗B7-H3 CAR构建体由抗 B7-H3 scFv、CD8 TM 区、4-1BB和CD3 ζ 胞内结构域组成。将CAR DNA序列插入到与ZsGreen 共表达的pLVX慢病毒载体中,随后产生慢病毒颗粒并转导入人NK-92MI细胞中,转到效率为24.9%。经过几轮分选,表达CAR的NK-92MI细胞百分比超过了95%。抗B7-H3 CAR的表达用qPCR检测,结果显示,与未转导的NK-92MI细胞相比,CAR在转导的NK-92MI细胞中高表达。
图1:B7-H3在肿瘤细胞系和原代人体组织上的表达
2. 携带抗B7-H3 CAR的NK-92MI细胞的生成
抗B7-H3 scFv由(G4S)3接头将抗B7-H3抗体8H9的轻链和重链可变区连接而成。抗B7-H3 CAR构建体由抗 B7-H3 scFv、CD8 TM 区、4-1BB和CD3 ζ 胞内结构域组成。将CAR DNA序列插入到与ZsGreen 共表达的pLVX慢病毒载体中,随后产生慢病毒颗粒并转导入人NK-92MI细胞中,转到效率为24.9%。经过几轮分选,表达CAR的NK-92MI细胞百分比超过了95%。抗B7-H3 CAR的表达用qPCR检测,结果显示,与未转导的NK-92MI细胞相比,CAR在转导的NK-92MI细胞中高表达。

图2:B7-H3 特异性CAR-NK-92MI细胞的生成 3. CAR-NK-92MI细胞对B7-H3阳性肿瘤细胞系的细胞毒性增强 为了确定B7-H3识别是否能提高NK-92MI的细胞毒性,我们通过 Calcein-AM实验比较了CAR-NK-92MI细胞和未修饰的NK-92MI细胞对一组人肿瘤细胞系的反应。结果显示,未修饰的NK-92MI细胞相比,CAR-NK-92MI细胞在所有E/T下的细胞毒性均显著增强。然而,对于MDA-MB-231,CAR-NK-92MI与未修饰的NK-92MI在1:1的低E/T下的有效性无显著差异,B7-H3阴性的Daudi细胞没有被任何NK-92衍生细胞裂解。未修饰的NK-92MI细胞对HCC827和MDA-MB-231 细胞系在高 E/T比下有中度杀伤作用,然而它们能被CAR-NK-92MI细胞裂解并具有显著性差异。这些细胞本质上对NK细胞敏感,与其他报道一致。总之,实验结果表明,CAR-NK-92MI细胞对B7-H3阳性肿瘤细胞具有特异性的细胞毒性。
 图3:B7-H3 CAR-NK-92MI 细胞对一组肿瘤细胞系的体外细胞毒性测定
4. CAR-NK-92MI细胞响应B7-H3阳性靶细胞的活化升高
NK细胞活化的一个标志是脱颗粒,其中裂解颗粒内容物(穿孔素和颗粒酶)被释放到靶细胞表面。CD107a、颗粒酶B、穿孔素是脱颗粒的三个主要标志物。为了进一步分析CAR-NK-92MI细胞的脱颗粒,我们通过流式细胞术分析了CD107a的表达和颗粒酶B、穿孔素的分泌。CAR-NK-92MI细胞分别与A549、NCIH23细胞以E/T为1:1共培养24h,结果显示,相比于未修饰的NK-92MI细胞,CAR-NK-92MI细胞表面CD107a的表达具有显著性差异。另外,B7-H3 CAR增强了在NK-92MI细胞脱颗粒中穿孔素、颗粒酶B的表达。在与靶细胞响应时,CAR-NK-92MI细胞中的颗粒酶B和穿孔素的水平显著上调。尽管A549细胞比NCIH23细胞表达更高水平的B7-H3,但是A549细胞中CD107a的水平似乎比NCIH23要低,这意味着溶细胞颗粒极化和脱颗粒不是由高于阈值的B7-H3密度决定的。我们假设不同受体控制两个细胞系的脱颗粒。因此,结果表明,脱颗粒激活在CAR-NK-92MI细胞的细胞毒性中起重要作用。
图3:B7-H3 CAR-NK-92MI 细胞对一组肿瘤细胞系的体外细胞毒性测定
4. CAR-NK-92MI细胞响应B7-H3阳性靶细胞的活化升高
NK细胞活化的一个标志是脱颗粒,其中裂解颗粒内容物(穿孔素和颗粒酶)被释放到靶细胞表面。CD107a、颗粒酶B、穿孔素是脱颗粒的三个主要标志物。为了进一步分析CAR-NK-92MI细胞的脱颗粒,我们通过流式细胞术分析了CD107a的表达和颗粒酶B、穿孔素的分泌。CAR-NK-92MI细胞分别与A549、NCIH23细胞以E/T为1:1共培养24h,结果显示,相比于未修饰的NK-92MI细胞,CAR-NK-92MI细胞表面CD107a的表达具有显著性差异。另外,B7-H3 CAR增强了在NK-92MI细胞脱颗粒中穿孔素、颗粒酶B的表达。在与靶细胞响应时,CAR-NK-92MI细胞中的颗粒酶B和穿孔素的水平显著上调。尽管A549细胞比NCIH23细胞表达更高水平的B7-H3,但是A549细胞中CD107a的水平似乎比NCIH23要低,这意味着溶细胞颗粒极化和脱颗粒不是由高于阈值的B7-H3密度决定的。我们假设不同受体控制两个细胞系的脱颗粒。因此,结果表明,脱颗粒激活在CAR-NK-92MI细胞的细胞毒性中起重要作用。
 图4:B7-H3 CAR-NK-92MI 细胞的脱粒和颗粒分泌
5. CAR-NK-92MI细胞在NSCLC移植瘤中的治疗效果
为了评估体内抗肿瘤活性,建立了A549细胞皮下模型。植入10天后,三组A549细胞移植瘤小鼠分别接受静脉注射CAR-NK-92MI细胞(5x10^6/剂)、未修饰NK-92MI细胞(5x10^6/剂)和PBS在第10、17、24、31天。结果显示,在实验结束时,相比于NK-92MI组和PBS组,CAR-NK-92MI组分别缩小肿瘤体积52.1%、63.8%。CAR-NK-92MI组的存活时间显著长于PBS组和NK-92MI组。因此CAR-NK-92细胞有效抑制肿瘤生长和荷瘤小鼠的生存期。
图4:B7-H3 CAR-NK-92MI 细胞的脱粒和颗粒分泌
5. CAR-NK-92MI细胞在NSCLC移植瘤中的治疗效果
为了评估体内抗肿瘤活性,建立了A549细胞皮下模型。植入10天后,三组A549细胞移植瘤小鼠分别接受静脉注射CAR-NK-92MI细胞(5x10^6/剂)、未修饰NK-92MI细胞(5x10^6/剂)和PBS在第10、17、24、31天。结果显示,在实验结束时,相比于NK-92MI组和PBS组,CAR-NK-92MI组分别缩小肿瘤体积52.1%、63.8%。CAR-NK-92MI组的存活时间显著长于PBS组和NK-92MI组。因此CAR-NK-92细胞有效抑制肿瘤生长和荷瘤小鼠的生存期。
 图5:用B7-H3 CAR-NK-92MI细胞治疗NSCLC异种移植瘤
实验结论:
在本研究中,我们构建了由4-1BB共刺激信号域和CD3ζ 结构域组成的第二代CAR,与目前临床使用的抗CD19 CAR-T细胞相似。本研究证实了抗B7-H3 CAR通过41-BB和CD3ζ 链的信号直接触发了NK细胞的溶解细胞功能。体外细胞毒性实验表明,CAR-NK-92MI细胞依据H7-B3的识别功能特异性地杀死肿瘤细胞。另外,CAR-NK-92MI细胞显著增强对所有B7-H3阳性细胞系的细胞毒性能力。抗B7-H3 CAR的重定向进一步增强了NK的活化和脱颗粒。脱颗粒是NK细胞活化的一个重要过程,它被触发脱颗粒释放溶解的颗粒分子,进而诱导靶细胞凋亡。除了穿孔素和颗粒酶B外,还观察到CD107a在CAR-NK-92MI细胞中显著上调。另外,在NSCLC移植瘤中,CAR-NK-92MI细胞显现出有效的抗肿瘤能力和延长荷瘤小鼠的生存时间。虽然CAR-NK-92MI缺乏长期的持久性,但是多次使用CAR-NK92MI细胞可以克服此缺点。因为辐射的CAR-NK-92MI细胞对于患者输注是确保安全所必须的,所以在CAR-NK-92MI细胞被应用于临床试验之前,我们需要进一步研究辐照对CAR-NK-92MI细胞内在特征的影响。
总之,B7-H3可作为NSCLC治疗的靶点。抗B7-H3 CAR-NK-92MI在体内和体外显示出显著的治疗效果。我们的研究支持开发CAR修饰的NK-92细胞作为过继癌症免疫治疗的一种选择。
图5:用B7-H3 CAR-NK-92MI细胞治疗NSCLC异种移植瘤
实验结论:
在本研究中,我们构建了由4-1BB共刺激信号域和CD3ζ 结构域组成的第二代CAR,与目前临床使用的抗CD19 CAR-T细胞相似。本研究证实了抗B7-H3 CAR通过41-BB和CD3ζ 链的信号直接触发了NK细胞的溶解细胞功能。体外细胞毒性实验表明,CAR-NK-92MI细胞依据H7-B3的识别功能特异性地杀死肿瘤细胞。另外,CAR-NK-92MI细胞显著增强对所有B7-H3阳性细胞系的细胞毒性能力。抗B7-H3 CAR的重定向进一步增强了NK的活化和脱颗粒。脱颗粒是NK细胞活化的一个重要过程,它被触发脱颗粒释放溶解的颗粒分子,进而诱导靶细胞凋亡。除了穿孔素和颗粒酶B外,还观察到CD107a在CAR-NK-92MI细胞中显著上调。另外,在NSCLC移植瘤中,CAR-NK-92MI细胞显现出有效的抗肿瘤能力和延长荷瘤小鼠的生存时间。虽然CAR-NK-92MI缺乏长期的持久性,但是多次使用CAR-NK92MI细胞可以克服此缺点。因为辐射的CAR-NK-92MI细胞对于患者输注是确保安全所必须的,所以在CAR-NK-92MI细胞被应用于临床试验之前,我们需要进一步研究辐照对CAR-NK-92MI细胞内在特征的影响。
总之,B7-H3可作为NSCLC治疗的靶点。抗B7-H3 CAR-NK-92MI在体内和体外显示出显著的治疗效果。我们的研究支持开发CAR修饰的NK-92细胞作为过继癌症免疫治疗的一种选择。
参考文献:Yang S, Cao B, Zhou G, Zhu L, Wang L, Zhang L, Kwok HF, Zhang Z, Zhao Q. Targeting B7-H3 Immune Checkpoint With Chimeric Antigen Receptor-Engineered Natural Killer Cells Exhibits Potent Cytotoxicity Against Non-Small Cell Lung Cancer. Front Pharmacol. 2020 Jul 30;11:1089. doi: 10.3389/fphar.2020.01089. PMID: 32848731; PMCID: PMC7406658.